Ley De Avogadro Ejercicios
En 1811 publicó una hipótesis en donde estableció. N1 0025 moles 2 l 05 l 01 moles.

Leyes De Los Gases Problemas De Quimica General Para Universitarios
FracV_1n_1 fracV_2n_2 que es otra manera de expresar la ley de Avogadro.

Ley de avogadro ejercicios. V1n1 V2n2 n1V1 n2V2 n1 n2 V1V2. Introducción a la químicaExercises resolved by applying Avogadros law for ideal gases. Ley de Avogadro Desarrollados 1- Cuál es la masa de 100 L de CO 2 en condiciones normales de presión y temperatura CN.
Biografía de Avogadro Ejercicios. Ejercicios Se Infla Un Globo Con 15 Litros De Helio A 560. El Mol Teoria Y Ejercicios Resueltos Química Paso A Paso.
Ley de avogadro 1. Esta ley de Avogadro establece que a condiciones normales o estándar temperatura de 0 C y 1 atm de presión un mol de gas ocupará un volumen de 224 litros. Si la cantidad molar aumenta al doble el volumen también se acrecentará en la misma proporción.
Ejercicio resuelto Ley de avogadro 2. Si variamos la cantidad de gas hasta un nuevo valor n 2 entonces el volumen cambiará a V 2 y se cumplirá. Fórmula de la ley de Avogadro.
El trabajo del científico italiano Amedeo Avogadro complementó los estudios de Boyle Charles y Gay-Lussac. Cuál es el volumen en litros que ocupan 498 g de ácido clorhídrico HCl g a T 52 C y P 11 atm. Respuesta 01 moles de helio habian.
Ley De Avogadro Parte 1 De 4. Supongamos que tenemos una cierta cantidad de gas n 1 que ocupa un volumen V 1 al comienzo del experimento. Ley De Los Gases Ideales Ejercicios Resueltos Paso A.
Esta ley fue descubierta por Avogadro a principios del siglo XIX. Ejercicio Resuelto FQ1BE2013 de Aplicación de la Ley de Avogadro para Química de Bachillerato. El volumen es directamente proporcional a la cantidad de gas.
Soluciones y Resoluciones de Ejercicios de Matemáticas Física y Química para Secundaria y Bachillerato. Establece la relación entre la cantidad de gas y su volumen cuando se mantienen constantes la temperatura y la presión. Explicación cinética de la ley de Avogadro.
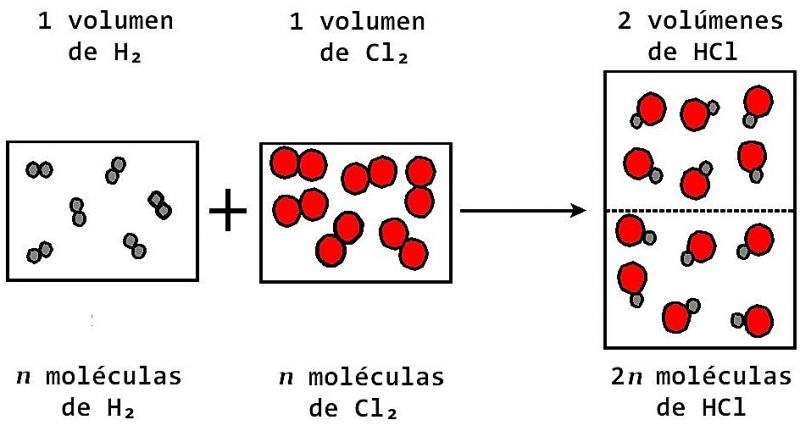
2 2 2 2 2 19 8 1 44 045 045 224 1 100 gCO molCO gCO mol mol L molCO LCO En condiciones normales 1 mol de cu alquier gas ocupa un volumen de 224 L posteriormente utilizando la masa molar del CO 2. A las mismas condiciones de presión y temperatura condiciones de Avogadro los volúmenes de dos gases están en la misma relación que sus números de. Ley de Avogadro Resueltos Ejercicio 1 Cuál es la masa de 100 L de CO 2 en condiciones normales de presión y temperatura CN.
Debido a que en el ejercicio anterior se mantienen constantes la presión y la temperatura y se relacionan el volumen con el numero de moles se puede emplear la ley de avogadro para solucionar este ejercicio. A Muxakara y otros 22 usuarios les ha parecido útil esta respuesta. Es decir que si se quieren estudiar un estado inicial y un estado final de un gas vale la fórmula.
2 2 2 2 2 198 1 44 045 045 224 1 100 gCO molCO gCO mol mol L molCO LCO En condiciones normales 1 mol de cualquier gas ocupa un volumen de 224 L posteriormente utilizando la masa molar del CO 2. Las primeras leyes de los gases fueron desarrollados desde finales del siglo XVII aparentemente de manera independiente por August Krönig en 1856 1 y Rudolf Clausius en 1857. V n K V volumen n número cantidad de moles.
Qué volumen ocupan 1x10⁶ de moléculas de Oxígeno O₂ en condiciones normales de presión y temperatura. Si continúas navegando por ese sitio web aceptas el uso de cookies. Las moléculas de O₂ se transforman a moles de moléculas de O₂ y por Ley de Avogadro los moles de moléculas pasan a litros del gas.
A partir de esta ley se puede deducir también que un mol de cualquier gas a. Amadeo Avogadro químico italiano 1776 1856 para explicar la ley de combinación quimica en fase gaseosa propuesto por Gay Lussac en 1811 planteó una hipótesis que actualmente se llama ley de Avogadro. Ejercicios resueltos aplicando la ley de Avogadro para gases ideales.
Para poder calcular el volumen que ocupa el gas de acido clorhídrico se debe conocer K para estas condiciones y el numero de moles n para esto vamos a realizar unos. 2 La constante universal de los gases se descubrió y se introdujo por primera vez en la ley de los gases ideales en lugar de un gran número de constantes de gases específicas descriptas por Dmitri Mendeleev en 1874. La cantidad de gas la medimos en moles.
Profeedi explica sobre la ley de Avogadro y cómo realizar cálculos de volumen y número de moles cuando la temperatura se mantiene constante. Ley de avogadro ejercicios LinkedIn emplea cookies para mejorar la funcionalidad y el rendimiento de nuestro sitio web así como para ofrecer publicidad relevante.
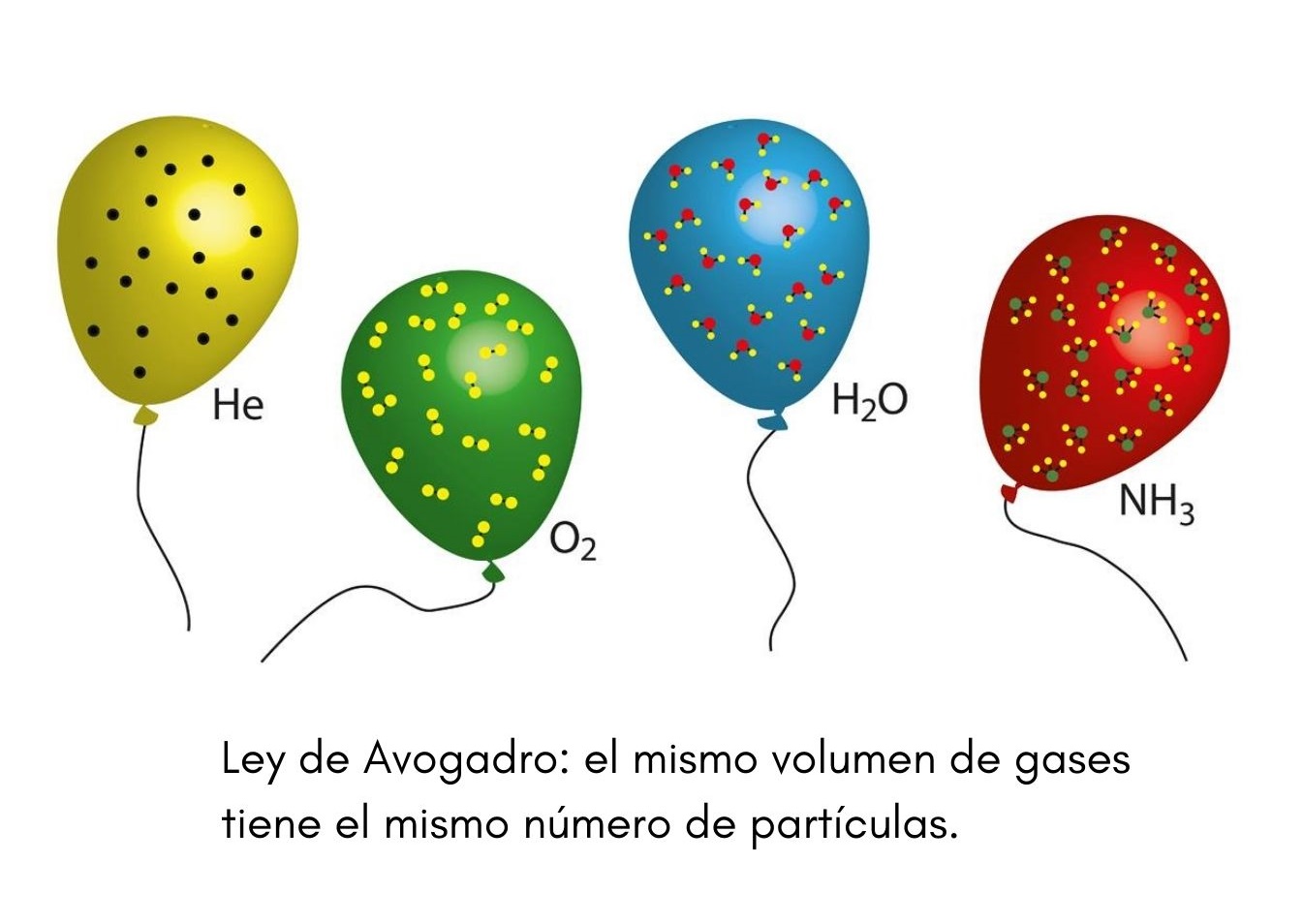
Ley De Avogadro Que Es En Que Consiste Enunciado Formula Aplicaciones

Ejercicios Propuestos Ley De Avogadro

Qm 1121 Ejercicios Resueltos De Gases Ideales
Ley De Avogadro Que Es Formula Condiciones Importancia Ejemplos

No De Avogadro Ejercicios Youtube

Fsica De 3 De Eso Leyes De Los

Ley De Avogadro Formula Y Ejemplos Quien Me Ayuda Brainly Lat

Ley De Avogadro Parte 1 De 4 Youtube

Ley De Avogadro Volumen Y Numero De Moles Explicacion Y Ejercicios Resueltos Lagu Mp3 Mp3 Dragon

Ejercicios Se Infla Un Globo Con 1 5 Litros De Helio A 560 Mm De Hg Si El Globo Se Eleva Hasta Alcanzar Una Altura Donde La Presion Es De 320 Mm Hg

Ley De Avogadro Parte 2 De 4 Youtube

Principio De Avogadro Explicacion Y Ejercicios Leyes De Los Gases Ideales Youtube

Ley De Avogadro Laquimicanosrodea











Posting Komentar untuk "Ley De Avogadro Ejercicios"